This content is also available in:
English
Português
Română
Türkçe
Schopnost screenovat p?evahou negativní cytologické preparáty a zaznamenávat p?íležitostné abnormality mezi mnoha tisíci bun?k vyžaduje specializovaný výcvik, znalost podstaty normálních a abnormálních bun?k a soust?ed?ní spolu se zaujetím. Zde se zabýváme zdroji chyb ve screeningu a jak jim p?edejít.
Zdroje chyb
Osobní d?vody
- Rutina, podv?domý proces, kterým mozek ignoruje nebo vypíná vzhledem k opakovaným vjem?m.
- Odvedení pozornosti telefonními hovory, jiným vyrušením nebo osobními myšlenkami, které mohou vést ke ztrát? pozornosti.
- P?ehnaná sebed?v?ra, zkušenost, že abnormální nález m?že být ?asto rozpoznán v prvním zorném poli m?že vést k p?ehlédnutí jednotlivých abnormálních bun?k.
- Neporozum?ní n?kterým jemným bun??ným zm?nám ve výcviku m?že vést k opakování takových chyb i u zkušen?jších screener?
- Screening p?íliš mnoha preparát? b?hem pracovního dne m?že vést ke ztrát? koncentrace
- Sp?ch na konci dlouhého pracovního dne m?že vést k p?ehlédnutí abnormalit.
- Úzkost z p?ehlédnutí abnormalit m?že vést k nadhodnocení benigních bun??ných zm?n jako atypických nebo hrani?ních.
Prost?edí a vybavení
- Neuspokojivá optika mikroskopu a ergonomie m?že vést k osobnímu dyskomfortu, který m?že ovlivnit výkon.
- Screeningové prostory neodd?lené od ostatních laboratorních ?inností
- Nedostate?né prostory pro preparáty, po?íta?e, záznamy a pod.
Známé p?í?iny falešn? negativních
- Malé, bledé a ?ídce p?ítomné bu?ky p?edstavují riziko p?ehlédnutí v primárním screeningu s konven?ními i LBC preparáty. (Demay 2000; Gupta et al. 2013; Leung et al. 2008; Mitchell & Medley1995).
- Hyperchromní nat?snané bun??né skupiny mohou být p?ehlédnuty a myln? považovány za endocervikální nebo endometriální bu?ky v konven?ních preparátech a LBC (Demay 2000; Gupta et al. 2013; Robertson & Woodend 1993).
- Glandulární abnormality chybn? interpretované jako reaktivní endocervikální bu?ky
- Nízká prevalence abnormálních bun?k v preparátech m?že redukovat citlivost screeningu (Evans et al. 2011).
Známé p?í?iny falešn? pozitivních a falešn? negativních nález?
Reaktivní a metaplastické zm?ny považované za dyskariózu
Endometriální bu?ky, histiocyty nebo lymfocyty chybn? interpretované jako neoplastické.
Zdroje chyb v primárním screeningu
|
Metody kontroly a zajišt?ní kvality
Výcvik a pokra?ující vzd?lávání cytologických screener? by m?lo být závazné pro všechny stupn? cytotechnolog? (QC).
Rychlý rescreening preparát? p?ed uvoln?ním nálezu je užite?nou metodou vnit?ní kontroly kvality doporu?enou v Evropských doporu?ených postupech. Ukázal se p?esn?jší než 10% úplný rescreening náhodn? vybraných (Wiener et al. 2007; Arbyn et al. 2003). Existuje n?kolik postup?:
Rychlý rescreening
Rychlý rescreening byl potvrzen jako ú?inná metoda redukce falešn? negativních po?t? v d?sledku únavy nebo chybné interpretace. (Faraker & Boxer 1996)
- Každý preparát je revidován 1 minutu ve zv?tšení 10x a abnormality jsou p?edávány vedoucímu cytotechnologovi nebo patologovi k uzav?ení nálezu.
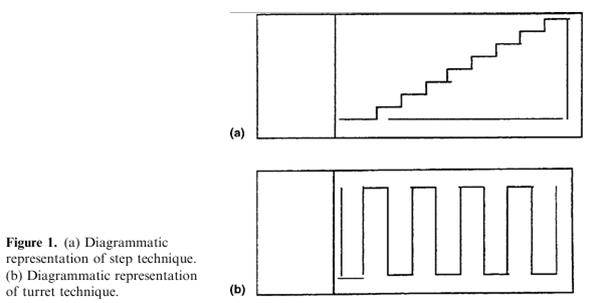
- Krokový screening byl prokázán Duddingem et al. (2001) jako efektivn?jší než screenování celého skla namátkou nebo v?žovit? (Obrázek 11.1). P?esnost se individuáln? lišila a klesala po víc než 50 vyšet?ených prepaprátech.
- Rychlý rescreening byl pprokázán jako efektivn?jší v redukci falešn? negativních po?t? než plný rescreening 10% preparát? (Manrique et al. 2006). Rychlý screening všech negativních a inadekvátních skel je doporu?enou metodou vnit?ní kontroly kvality v UK, bu? jako rescreening nebo prescreening (NHSCSP 2013).
Rychlý prescreening
Rychlý prescreening všech preparát?, než jdou do rutinního screeningu (abnormální bu?ky jsou zaznamenány, ale nejsou ozna?eny v preparátu) se ukázal stejn? citlivý jako rychlý rescreening (Arbyn et al. 2003).
- Prescreening má výhodu, že lze monitorovat jeho citlivost (k finálnímu výsledku) v porovnání s plným primárním screeningem.
- Rychlý prescreening je zajímav?jší a uspokojiv?jší než rescreening negativních preparát?, protože jde o zjišt?ní v?tšího po?tu abnormálních bun?k, což m?že pozitivn? ovlivnit citlivost (Evans et al. 2011).
- Prescreening byl prokázán jako citliv?jší v LBC než v konven?ních nát?rech (Dudding et al. 2011a) a jeho citlivost se v ?ase m?že lepšit (Dudding et al. 2011b).
Automatizovaný screening
Automatizovaný screening je nákladný, ale m?že poskytnout ješt? p?esn?jší nástroj kontroly kvality, pokud je využit jako prescreeningová metoda sledovaná plným primárním screeningem (Heard et al. 2013). Na rozdíl od rychlého rescreeningu nebo rychlého prescreeningu, screening s automatizovaným systémem je minimáln? stejn? citlivý jako plný primární screening (Roberts et al. 2007) a byl pro tento ú?el akreditován.
Stanovení personálního a laboratorního výkonu v primárním screeningu
Rychlá revize, rychlý prescreening a 10% plný rescreening p?edstavují nástroje pro interní a externí zajišt?ní kvality personálního a laboratorního výkonu v primárním screeningu, které jsou kritickými kroky procesu, pokud cytologie je použita jako primární screeningový test, nebo jako t?íd?ní po primárním HPV screeningu.
Citlivost primárního screeninguPo?et screenovaných jako abnormální x 100
___________________________________________________________
Po?et abnormálních finálních nález? (ASC-US+ nebo HSIL+)
|
Všechny tyto metody rescreeningu nebo prescreeningu detekují abnormality, než je uvoln?n nález, ale odhalují velmi málo dodate?n? zjišt?ných abnormalit: 0.18% (CI 0.14-0.21%) pro rychlý rescreening a 0.19% (CI 0.03-0.35%) pro rychlý prescreening (Arbyn et al. 2003). Tento mírný nár?st v citlivosti poskytuje mohutný nástroj pro stanovení výkonu cytologických screener?, ale m?ly by být hodnoceny v kontextu dalších faktor?.
- Dalšší postup uu chyb ve screeningu by m?l být d?v?rný a citlivý s v?domím, že i nejzkušen?jší screener m?že ojedin?le minout high-grade abnormality.
- Nápravná opat?ení, nap?. dodate?né školení by m?ly být využity pouze v p?ípad? nálezu systematických chyb.
- Protože výsledná zpráva záisí na p?esnosti patologa, citlivost screeningu by m?la být posuzována v kontextu individuálních variací ve struktu?e nález? v laborato?i.
- Okrajové d?vody pro špatný výkon, nap?. p?ílišné pracovní zatížení , špatné vybavení a nedostate?né laboratorní podmínky by m?ly být ?ešeny odpovídajícím zp?sobem.
QC a QAf primárního screeningu
|

