This content is also available in:
English
Italiano
Português
Deutsch
Čeština
Română
Sitolojik örneklerin i?lenmesi süreci; spesimen ve istek formunun kabulünü, mikroskopik inceleme için lamlar?n haz?rlanmas?n?, boyanmas?n?, taranmas?n? ve raporlanmas?n? kapsar. Tüm bu süreçlerde, kalite kontrol ve kalite güvence önlemlerinin uygulanmas? çok önemlidir.
Örnekler ve istek formlar?n?n kabulü
- Örnek ve istek formu kar??la?t?r?larak kontrol edilir
- Örnek üzerinde ve formda hastay? tan?mlay?c? en az üç tane bilgi bulunmal?d?r (ad?, soyad?, do?um tarihi, sa?l?k sigorta numaras?, hastane numaras?).
- Laboratuvar?n referans numaras? verilir
- Hasta kimlik ve örnek referans numaras? laboratuvar?n bilgi yönetim sistemine kaydedilir (LBYS).
Mikroskopik inceleme için lamlar?n haz?rlanmas?
- S?v? bazl? lamlar, cihaz?n ve üreticinin talimatlar?na uyularak haz?rlan?r. En s?k kullan?lan yöntemler, ThinPrep (Hologic) ile SurePath’dir ve hangisi kullan?lacaksa laboratuvar içinde el kitab? bulunmal?d?r. ThinPrep ekipmanlar? ve örnekleme metodlar?n?n ilgili linkleri, ana web sitesinde verilmektedir: http://www.thinprep.com/hcp/ifu/
- BD SurePath için link adresi: http://www1.bd.com/anz/training/surepath
Papanicolaou yöntemi kullan?larak boyama
- Otomatik boyama makinelerinde kullan?lan ‘regresiv’ Papanicolaou yöntemi, Tablo 8’de gösterilmi?tir
- Tüm slaytlar monte, lamelle kapl? ve etiketlidir
- Her bir hücre çekirde?inin boyanma ve z?t boyanma özellikleri günlük kontrol edilir.
Papanicolaou boyama yöntemi
Dr.Papanicolaou, y?llar?n deneyimlerinden sonra bir Trikrom boyas? geli?tirdi ve bu boya (biraz de?i?tirilmi? hali ile) günümüzde halen kullan?lmaktad?r. Trikrom boyas?; bir nükleer boya ile hematoksilen ve iki z?t boyan?n (OG-6 ve EA-50) bir birle?imidir. OG-6 keratini boyarken; EA-50 (eosin ve azure’dan olu?an çiftli boya) skuamöz epitel hücrelerinin sitoplazmas?n?, nükleolü ve k?rm?z? kan hücrelerini boyar.
Optimal boyama için; lamdaki hücrelerin üzerinde istenmeyen kuruma artefaktlar?n?n olu?mamas? için, fiksasyondan önce ya da i?lem s?ras?nda hücrelerin kurumas?na izin verilmemelidir. Her laboratuar kendi renk dengesini sa?lamak için, boya modifikasyonlar?n? s?kl?kla yapar: uyarlamalar s?kl?kla hematoksilen ve EA-50 boyalar?n?n boyama sürelerini de?i?tirerek yap?l?r.
Musluk suyunun kimyasal içeri?i, ortam s?cakl???, örne?in pH’? ve her seferinde boyanan lamlar say?s? gibi basit varyasyonlar; boyan?n renk dengesini etkileyebilir. Sitolojik tan?larda tutarl?l??? kolayla?t?rmak için, kalite kontrol yöntemleri ile boyama dengesinin tutarl?l???n? sa?lamak laboratuvarlar?n görevidir. Nükleer detay?n net bir ?ekilde tan?mlanmas? ve sitoplazma berrakl???n?n korunmas? ?art?yla, renk dengesinde laboratuvarlar aras? de?i?kenlikler kabul edilebilir.
?leriye do?ru(progresiv) veya geriye do?ru(regresiv) boyama
Progresiv (ileriye do?ru) boyama yönteminde; çekirdek haematoksilen ile istenen yo?unlukta boyand?ktan sonra nükleer boyaman?n yo?unlu?u, bir “mavile?tirici (blueing)” madde içine lam dald?r?larak kontrol edilir. En s?k kullan?lan ‘blueing’ maddesi, Scott’?n musluk suyudur (pH 8.02). ?leriye do?ru boyama, sitoplazmay? çok hafif renklendiriyor.
Geriye do?ru (regresiv) boyama yöntemi kullan?l?rken; çekirdekler bilinçli olarak, asidik olmayan hematoksilenle fazla boyan?rlar. Fazla boya, seyreltik hidroklorik asit çözeltisi ile uzakla?t?r?l?r (asitli su). Soldurma i?lemi daha sonra, akan musluk suyuna lamlar?n bat?r?lmas?yla durdurulur. Soldurma(de-staining) i?lemi, hiperkromatik bir çekirde?in hipokrom hale dönmesine yol açabilece?inden, geriye do?ru yöntemde zamanlaman?n kritik önemi vard?r.
Papanicolaou boyas?nda, de?i?kenlik faktörleri olarak; kullan?lan boyama yöntemi yan?s?ra boyalar?n ticari markas? ve hücresel örne?in pH’?n? da hat?rlatmak isteriz. Sonuç olarak; Papanicolaou boyas? tam bir ‘stoikiyometrik’ boya olarak kabul edilemez.
Her iki yöntem de çal???r ve laboratuvara ba?l? olarak bu yöntemlerden herhangi biri kullan?labilir. Genel boyama sonuçlar? ve tan?sal kapasiteleri benzerdir.
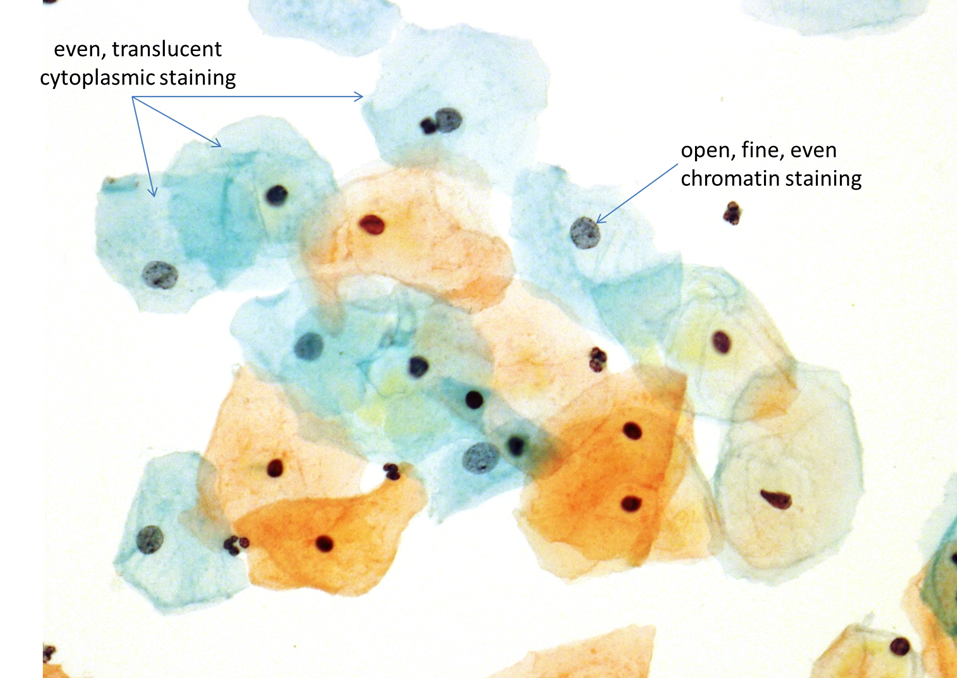
Papanicolaou boyamas?n?n özellikleriHer bir çekirdek;
Z?t boyalar (sitoplazma)
Boyalar?n yo?unluklar? e?it olmal?d?r Nükleer boyanma ile keskin bir kontrasta sahip bir sitoplazmik saydaml?k olmal?d?r |
Tablo 8.1. Regresif Papanicolaou boyama yöntemi (Otomatik boyama makinesi için)
|
?stasyon |
Solüsyon |
Zaman (dakika) |
|
1 |
%95 alkol |
1:30 |
|
2 |
%70 alkol |
1:30 |
|
3 |
Hematoksilen |
4:00 |
|
4 |
Asit su |
0:05 |
|
Y?kama 1 |
Su |
Y?kama |
|
Y?kama 2 |
Su |
Y?kama |
|
Y?kama 3 |
Su |
Y?kama |
|
Y?kama 4 |
Su |
Y?kama |
|
5 |
%70 alkol |
2:00 |
|
6 |
%95 alkol |
1:00 |
|
7 |
OG6 |
2:00 |
|
8 |
%95 alkol |
0:10 |
|
9 |
%95 alkol |
0:10 |
|
10 |
EA50 |
6:00 |
|
11 |
%95 alkol |
0:15 |
|
12 |
%95 alkol |
0:15 |
|
13 |
Absolü alkol |
1:00 |
|
14 |
Absolü alkol |
1:00 |
|
15 |
Absolü alkol |
1:00 |
|
16 |
Ksilen |
3:00 |
|
17 |
Ksilen |
2:00 |
|
Ç?k?? |
Ksilen |
1:00 |
Tarama ve sitolojinin raporlanmas?
- Bir sitoteknolog veya sitoloji taray?c?s? lamlar? tarar.
- Kurumsal protokollere ba?l? olarak; negatif ya da yetersiz olarak de?erlendirilen tüm lamlar, h?zla yeniden gözden geçirilir (rapid review) ve herhangi bir anormallik gözlendi?inde, daha k?demli bir sitoteknolo?a de?erlendirmesi için yönlendirilir.
- Negatif ve yetersiz sonuçlar, kurumsal protokollere göre taray?c?lar taraf?ndan imzalan?r,
- Tüm anormal sitoloji lamlar? ise kurumsal protokollere de ba?l? kal?narak, nihai rapor için bir dan??man patolo?a, k?demli bir bilim insan?na ya da bir biyomedikal uzman?na yönlendirilir.
- Nihai rapor; imzalan?r, kaydedilir ve posta yolu ile veya elektronik olarak yaymay? alan ki?iye gönderilir.
- Nihai rapor; hastan?n yönetimi için öneriler içerir, bunlar kolposkopik muayene önerilmesi veya örnek yetersiz ise yayma testinin tekrar? olabilir.
- E?er önerilmi?se, ASC-US ile dü?ük dereceli epitelyal hücre anormalli?inin triyaj?nda veya CIN tedavisi sonras?nda kür testi olarak HPV testi yap?l?r.
- Hasta, testinin sonucu hakk?nda bilgilendirilir.
- Klinisyen veya örne?i alan klinik, anormal sitolojik sonuç durumunda gerekli ad?mlar? atmakla sorumludur.
- Kolposkopi randevular? ve tekrar testleri için bir hat?rlatma sistemi kurulmal?d?r.
Bu prosedürler; laboratuvarlar, bölgeler ve ülkeler aras?nda de?i?kenlik gösterebilir, ancak servikal kanser taramas?n?n kalite güvencesi hakk?ndaki Avrupa k?lavuzlar?na uyulmal?d?r (Wiener ve ark.).
Konvansiyonel ve s?v? bazl? sitoloji ile tarama protokolleri
Kalite kontrol yöntemlerini de içeren tarama ve raporlama protokolleri; bölümdeki dan??man patologlarla i?birli?i içinde laboratuvar yöneticisi taraf?ndan uygulanmal?d?r.
Deneyimlerini geli?tirmek amac?yla, sitoteknologlar geni? bir yelpazede lam çe?itlili?i olan olgular? görmelidir. Laboratuvarlar y?lda en az 15.000 servikal yaymay? de?erlendirmelidir ve her bir taray?c?n?n, düzenli molalar ile birlikte, günde 50 konvansiyonel veya 80 SBS yaymay? taramas? beklenebilir. Taray?c?n?n kendi çal??ma alan? ile binoküler mikroskopu bulunmal? ve y?lda en az 3000 olguyu taramas? hedeflenmelidir.
Haz?rlanan slaytlar, x10’luk objektif ve x10’luk oküler kullan?larak anormal hücreler aç?s?ndan taranmal?d?r; tüm slayt? taramak için de ayn? objektif kullan?lmal?d?r. Taray?c?, lamel alt?ndaki tüm alan? detayl? bir ?ekilde incelemelidir. Taramaya genellikle lam?n en kö?esine gelinerek ba?lan?l?r ve ad?m ad?m lam ilerletilerek, lamelin kaplad??? tüm alan tamamlanana kadar devam edilir.

Bir taray?c?n?n; x10’luk bir objektif kullanarak, bir lam? tarama i?lemi s?ras?nda yakla??k 250-300 görme alan?n? inceledi?i tahmin edilmektedir. Konvansiyonel sitolojide bu süreci tamamlaman?n ortalama süresi 6-10 dakikad?r (aral??? 5 -20 dakika)
Taray?c?n?n görevi, servikal yaymadaki ilgili hücreleri i?aretlemektir. ??aretler veya noktalarken x 4’lük objektif kullan?lmal?d?r. ??aretleme protokolleri, laboratuvarlar taraf?ndan kararla?t?r?lmakla birlikte normalde SBS tarand???nda, renkli uçlu keçeli kalem, konvansiyonel yayma i?aretlenirken ise beyaz mürekkepli i?aretleme kalemi kullan?l?r. ?lgi çekici alanlar? veya hücreleri detayl? olarak incelerken x20’lik veya x40’l?k objektif kullan?lmal?d?r.
Her bir yaymada sitoloji talep formu bulunmal? ve kad?n?n servikal tarama öyküsü yaymay? incelemesinden önce sitolog taraf?ndan gözden geçirilmelidir.
ThinPrep lam?n? tarama protokolleri
- Konvansiyonel yaymadan s?v? bazl? sitolojiye dönü?üm sürecinde sitologlar, laboratuvarlar?nda kullan?lan teknolojiye (ThinPrep/ Surepath) yönelik e?itim almal?d?r.
- ThinPrep; konvansiyonel yayman?n fiksatifi olan etanol-bazl?dan farkl? olan metanol-bazl? fiksatif kullanmaktad?r. ThinPrep lamlar?nda nükleer detay iyi korunmu?tur; ancak nükleer membran?n daha belirgin olmas?, immatür skuamöz metaplazi ile HSIL aras?ndaki ay?r?c? tan?da daha dikkatli olmay? gerektirir. ThinPrep lamlar?, taray?c?n?n tercihine ba?l? olarak, yatay ya da yukar?dan a?a??ya dü?ey düzlemde yap?labilir.
- H?zl? inceleme (rapid review) veya ön inceleme (pre-view) ile ilgili bir k?lavuz henüz bulunmamaktad?r.
SurePath lam?n? tarama protokolleri
- Konvansiyonel yaymadan s?v? bazl? sitolojiye dönü?üm sürecinde sitologlar, laboratuvarlar?nda kullan?lan teknolojiye (ThinPrep/ Surepath) yönelik e?itim almal?d?r.
- SurePath’de kullan?lan fiksatif, konvansiyonel yayma için kullan?lan etanol-bazl? fiksatifle ayn?d?r.
- SurePath’in lamlar?nda taranacak hücre alan? Thin-Prep’e göre daha küçük çapl? olmas?na ra?men, lam?n taranmas? için geçen süre daha k?sa olmamaktad?r çünkü SurePath preparatlar?, tek tabaka halinde da??lmazlar ve üç boyutlu hücre gruplar?na büyük büyütmede, yukar? a?a?? taramalarla odaklan?lmas? gerekmektedir
S?v? bazl? sitoloji için e?itim
|

