This content is also available in:
English
Português
Deutsch
Il Pap test è stato sviluppato dal dottor George Papanicolaou, un anatomista americano che nacque e si formò in Grecia e si occupò della ricerca riguardante gli effetti degli ormoni ovarici sull’epitelio del tratto genitale femminile.
Nel 1926, il dott. Papanicolaou notò che le cellule tumorali potevano essere viste nelle secrezioni vaginali delle donne con tumoure cervicale, portando alla sua pubblicazione Diagnosi del tumoure uterino con lo striscio vaginale nel 1943. Il primo ambulatorio per lo screening del tumore cervicale fu aperto in Massachusetts nel 1945.

La Citologia come test di screening – il Pap test
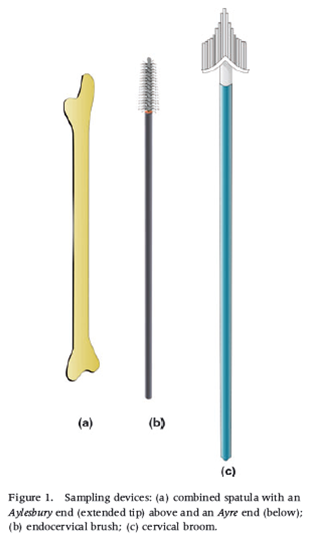
Lo striscio cervicale, o Pap test, è stato sviluppato come un esame semplice, poco costoso e sensibile, che è stato usato in tutto il mondo come test di screening per più di 50 anni. Solo in UK, vengono fatti più di 3 milioni di strisci cervicali all’anno. L’esame viene effettuato sfregando gentilmente la superficie della cervice e prelevando un campione di cellule epiteliali usando una spatola, uno spazzolino o un altro mezzo di campionamento.
In citologia convenzionale, le cellule sono direttamente trasferite dalla spatola o dallo spazzolino, al vetrino e poi fissate usando un fissativo spray o alcool. Attualmente noi utilizziamo la liquid-based cytology come metodo preferenziale di raccolta del campione perchè permette al laboratorio di produrre i propri vetrini e, contemporaneamente, avanzare del materiale per ulteriori test. Qualunque metodo venga utilizzato, il prodotto finale sono delle cellule sottilmente distribuite su un vetrino per la valutazione microscopica.
Screening citologico
Il primo esame microscopico viene effettuato da un citotecnologo (screener primario) che è formato per identificare cellule anormali tra molte migliaia di cellule normali nello striscio o nella preparazione in fase liquida. I campioni che contengono cellule patologiche sono passati ad un senior scientist o a un patologo che grada le anormalità in base ad un sistema terminologico riconosciuto e fornisce raccomandazioni ai clinici sul management del paziente.
Questo test semplice e poco costoso ha salvato innumerevoli vite da quando è stato introdotto grazie al trattamento delle lesioni pre-invasive.
Il Pap test come parte di in programma di screening nazionale
Lo scopo primario del Pap test è quello di prevenire lo sviluppo di un tumoure infiltrante tramite la scoperta di lesioni pre-cancerose conosciute come neoplasia intraepiteliale cervicale (CIN) nella cervice uterina, che di solito sono asintomatiche e individuate solo con lo screening. Il trattamento conservativo del CIN con l’ablazione locale o la rimozione dell’epitelio anormale riduce in modo significativo il rischio di malattia infiltrante.
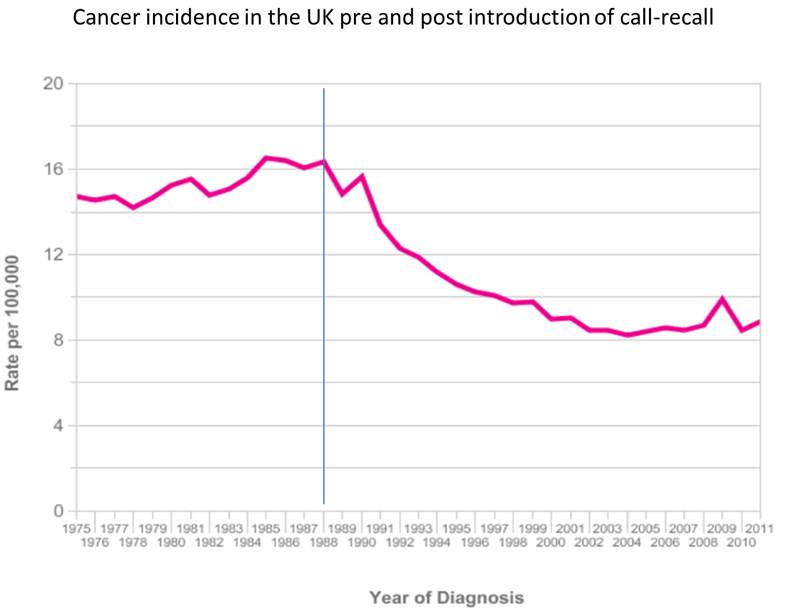
La neoplasia occulta, prima che diventi visibile e, di solito, ad uno stadio precoce e trattabile, può essere individuata dallo screening citologico [Link al capitolo 4 – Patogenesi del tumore cervicale e dei suoi precursori]
Sebbene alcuni test citologici siano talvolta effettuati durante l’esame di donne che sono già sintomatiche o hanno un tumore già clinicamente evidente, questi test potrebbero non essere affidabili. C’è un rischio maggiore che il campione citologico venga refertato come negativo o inadeguato, a causa della contaminazione con sangue, cellule infiammatorie e necrosi associati al tumore infiltrante, che oscurano le cellule patologiche nello striscio. [Link al capitolo 8 – Raccogliere e processare i campioni dalla cervice]
Donne con sintomi o segni che suggeriscano una neoplasia infiltrante dovrebbero essere inviate per un esame ginecologico qualsiasi sia il risultato del test.
Il ruolo del papillomavirus umano (HPV)
La scoperta dell‘HPV come principale agente eziologico del tumore della cervice uterina e dei suoi precursori, ha rivoluzionato lo screening e il ruolo della citologia nel processo di screening.
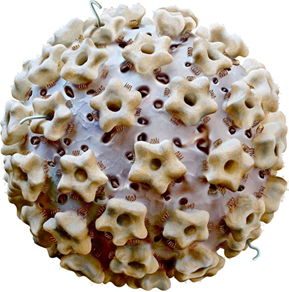
Il test dell’HPV è attualmente raccomandato per la selezione di donne con una citologia atipica/borderline e durante il follow-up dopo il trattamento per un CIN (test di cura). Sebbene la citologia sia un metodo sensibile per identificare la ricomparsa di malattia, le donne che sono state trattate per un CIN di alto grado hanno un rischio aumentato di sviluppare una neoplasia e il test dell’HPV è più sensibile che la citologia da sola.
In molti paesi, lo screening primario di HPV è stato introdotto perchè è stato dimostrato essere più sensibile della citologia nell’identificare i CIN di alto grado, sebbene la sua specificità sia sostanzialmente più bassa. Questo fondamentalmente modifica il ruolo della citologia da screening a test diagnostico. Comunque non cambia i principi della citologia cervicale o la vitale importanza del controllo di qualità.
Trattamento delle lesioni precancerose
All’inizio dello screening, il trattamento era riservato al carcinoma in situ, attualmente chiamato neoplasia intraepiteliale cervicale di grado 3 (CIN3). Coni e isterectomie erano gli unici trattamenti disponibili.
Ablazione e rimozione del CIN e della zona di trasformazione sono stati sviluppati durante gli anni ’90 come terapia più conservativa ma altamente efficace: larga escissione con loop della zona di trasformazione ( LLETZ). La LLETZ è attualmente l’intervento di scelta, sebbene anche cone biopsy, cervicectomia e isterectomia possano essere effettuate per lesioni diffuse, neoplasie ghiandolari e tumori infiltranti occulti.
Evitare i rischi del trattamento che sono collegati alla profondità delle biopsie escissionali, rappresenta una preoccupazione nello screening cervicale.
Vaccinazione per HPV
Lo sviluppo e l’introduzione della vaccinazione per l’HPV, che è stata approvata come vaccino nel 2005, rivoluzionerà ulteriormente la pratica della citologia cervicale, della colposcopia e del trattamento delle lesioni pre-neoplastiche del tumore della cervice. Le donne vaccinate sono già entrate nei gruppi in età da screening in alcuni paesi, come l’Australia, e sono stati già registrati gli effetti previsti di ridurre la prevalenza dei condilomi genitali e CIN.
Come risultato della diminuzione della prevalenza di CIN e cancro, l’accuratezza della sensibilità dello screening citologico e del suo valore predittivo positivo, potrebbe essere compromessa, che è uno dei motivi principali per cui il test per HPV è stato introdotto in molti paesi. Allo stesso modo, la bassa specificità del HPV test richiede la citologia come test diagnostico di smistamento – evidenziando ulteriormente la vitale importanza del controllo di qualità.
Learning points del capitolo 1:
|

